Адиабатно процес - studopediya
Основните параметри, които характеризират състоянието на налягането на газа P. е обем V и температура T. Връзката между тези параметри за идеалната избран Менделеев-Clapeyron уравнение:
където М - масата на един мол от газ, кг / мол; m - маса на газ, кг; Т - абсолютна температура на газа, K; R = 8,31 J / (мол х К), - константа на универсалната (моларен) газ.
Ако има две от трите основни параметри на газа, третата може да се изрази чрез тях. При смяна на три параметри на началните параметри газ (p1. V1. Т1), свързани с нови параметри на същото количество газ (Т2 p2. V2.) Уравнение.
Адиабатно преработвателната процес, който протича без топлообмен с околната среда. т.е. Q = 0.
Адиабатен процес може да се проведе в системата, заобиколен от топлоизолиращ (адиабатно) обвивка. Един пример за този процес - работния цикъл на двигателя топлина, при което газ (пара) в цилиндъра разширява с топлоизолационни стени и буталото, при липса на необратими трансформации на работа на триене в топлина. Адиабатен процес може да се осъществява в отсъствие на адиабатно обвивка; за това той трябва да се процедира толкова бързо, че се е случило по време на процеса на пренос на топлина между системата и околната среда.
Първият закон на термодинамиката е:
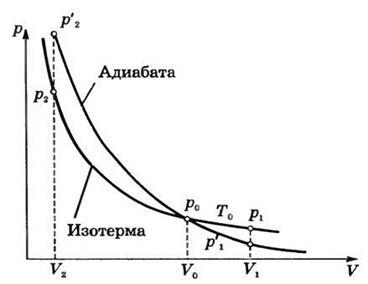
Това означава, че когато адиабатен процес, системата може да изпълнява работата по външни органи само чрез загубата на своята вътрешна енергия. Ако А> 0, # 916; U = -А <0, т.е. U2 Както е известно, газ извършва работа, ако # 916; V> 0. По този начин, когато адиабатно разширение газ извършва работа се се охлажда. Обратно, ако адиабатен компресия (А <0 ) над газом совершается работа и газ нагревается . Когато адиабатно налягане процес и обем са свързани чрез уравнението: р х V г = конст или р х Т г / (г - 1) = конст, където # 947> 1 - съотношението на специфичните топлини (или съотношение на Поасон). Това уравнение се нарича адиабатно уравнението или уравнението на Поасон. S ентропия промяна на системата в обратима адиабатен процес поради трансфера на топлина през границата на системата не се осъществява: Където Т - температура на системата, # 948; Q - топлина, получена от системата. Благодарение на този адиабатен процес може да бъде част от по-обратим цикъл. Адиабатно промяна на състоянието на газа може да се изрази графично. Графиката на този процес се нарича адиабатно (фиг. 2). При същите първоначалните условия (p0. V0) намалява по-бързо в адиабатно разширение на налягането на газ, отколкото при изотермични, поради спадане на налягането, причинено не само чрез увеличаване на обема (както в изотермично разширяване), но също така и намаляване на температурата. Затова той отива по-долу адиабатно и изотермичен газ при адиабатно разширение прави по-малко работа, отколкото в разширяването на изотермичен.
С бързото компресия (разрастване) на топлина няма време да се появят и процеси могат да бъдат считани адиабатно (nonequilibrium). Следователно, всеки газ се нагрява чрез бързо компресия (например, термопомпа при надуване на велосипедни гуми). Ако силно и бързо температура на пресоване може да се повиши, така че в присъствието на бензинови изпарения във въздуха се запалва. Това се използва в дизелови двигатели за запалване на горивния смес. Това обяснява необходимостта от специална охлаждане мощни компресори.
Охлаждащ въздух под адиабатно разширение причинява образуването на облаци.